
近日,我室李继喜课题组在炎性坏死(细胞焦亡)作用机理研究方面取得重要进展,研究论文以《Structure insight of GSDMD reveals the basis of GSDMD autoinhibition in cell pyroptosis》为题发表在国际著名期刊《美国科学院院报》(Proc Natl Acad Sci U S A)上。
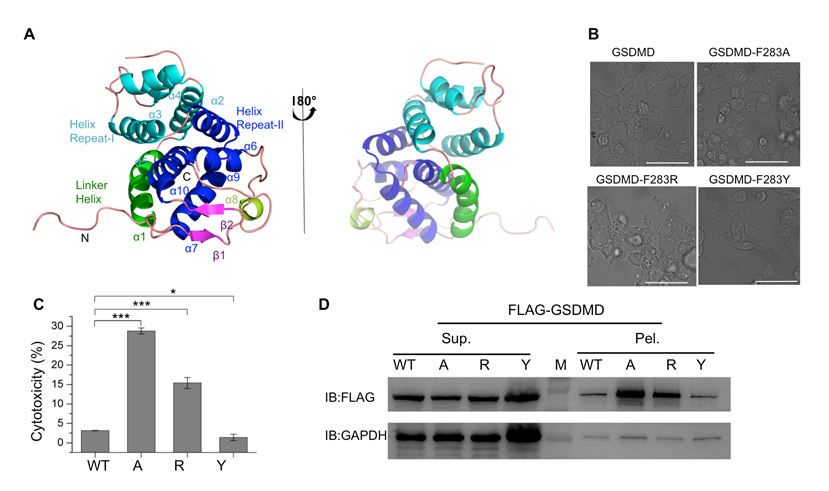
图注:细胞焦亡蛋白GSDMD-C的三维结构(A)及关键氨基酸残基突变对细胞存活的影响(B-D)
细胞焦亡是机体在感知病原微生物侵染后启动的免疫防御反应,在拮抗和清除病原感染危险信号中起着重要的作用。细胞焦亡本质上是由GSDMD(gasdermin D)蛋白介导的细胞炎性坏死,与多种病理生理过程紧密相关。一旦发生,GSDMD蛋白的N-端高聚并与脂类结合,在细胞膜上形成孔洞,细胞逐渐膨胀至细胞破裂,最终大量细胞内含物如IL-1β释放,激活强烈的炎症反应。但是目前尚缺乏GSDMD蛋白高分辨率三维结构信息,从自抑制状态到活化状态的构象变化也不清楚。
李继喜团队通过X-光晶体衍射方法解析了GSDMD-C的三维精细结构,并结合X-射线小角衍射和动态光散射等技术分析了GSDMD的溶液结构及物理化学性质。研究发现GSDMD-C的第一段柔性区域深入到GSDMD-N结构域中,对GSDMD的稳定性起着很大作用。基于三维结构的定点突变及替换实验表明该区域对于细胞存活至关重要。表面电荷分布表明,与C端结构域分开后,GSDMD的N端结构域表面暴露出来,通过正负电荷之间的相互作用,进一步寡聚从而引起细胞焦亡。该研究成果阐明了GSDMD蛋白的自抑制结构基础,有助于我们进一步理解GSDMD在炎性细胞坏死发生中的作用机理,并为将来筛选治疗败血症等相关疾病的候选药物提供研究基础。
硕士研究生匡思运和郑军为本文的共同第一作者,李继喜教授为本文通讯作者。李继喜课题组主要从事病原体-宿主天然免疫应答相关蛋白质复合物的结构基础与分子机制研究。自2014年加入复旦大学后,已在Immunity、PNAS、Annu Rev Immunol、Sci Rep等期刊上发表多篇研究论文。该研究得到了科技部国家重点研发计划、国家自然科学基金委、上海市东方学者等项目的资助。
全文链接:http://www.pnas.org/content/early/2017/09/18/1708194114.full.pdf