
足够的营养是细胞增殖和组织发育的必要条件。细胞增殖和组织发育需要上调组蛋白乙酰化来激活基因转录。二者之间的联系,也就是:“营养物信号如何被传递到组蛋白乙酰化?”这个基础生物医学问题,长期未能得到阐明。
第2021年6月17日,我室赵世民团队联合复旦大学生物医学研究院徐薇团队合作在Nature Metabolism杂志上发表文章Nuclear dihydroxyacetone phosphate signals nutrient sufficiency and cell cycle phase to global histone acetylation,发现代谢物信号和细胞周期信号共同调控组蛋白乙酰化,实现基因转录激活。

在营养代谢物丰富的条件下,细胞内的富营养感知器mTORC1信号被激活,使细胞处于可以进行合成代谢和增殖的状态。然而,细胞并不是随时可以增殖,只有当细胞处于第一间歇期(G1期)时,细胞才能够合成积累增殖所需的合成原料。mTORC1信号因此将富营养信号传递给细胞周期依赖性激酶2 (Cyclin-dependent kinases, CDK2) 。由于CDK2只在G1期出现,因此富营养信号只在G1期被传递到细胞核内,参与组蛋白乙酰化和转录激活。
接收了富营养信号的CDK2并不直接进入核内,它通过磷酸化名为磷酸丙糖异构酶 (TPI1) 的糖酵酶并将其引入细胞核。进入核内的TPI1可以通过生成全新的代谢物乙酰磷酸二羟丙酮 (Acetyl-DHAP,dihydroxyacetone phosphate)来降低DHAP对组蛋白去乙酰化的促进,进而导致组蛋白乙酰化和基因转录的激活,实现细胞增殖 (下图)。
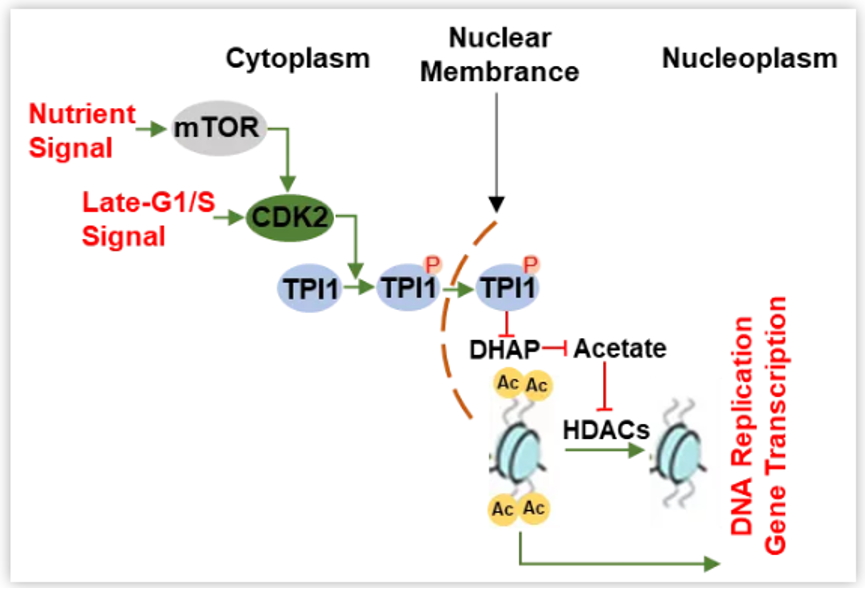
该研究发现了一条可以整合营养信号、细胞周期信号和转录激活通的全新信号通路,为代谢环境改变细胞表观性状调控细胞增殖揭示了全新机理,也为包括癌症等代谢失调相关疾病的干预提供了新思路。
赵世民团队长期从事蛋白质乙酰化研究,原创发现了蛋白质乙酰化是代谢调控新机制(Science 2010a, Science 2010b),蛋白质乙酰化调控葡萄糖平衡(Molecular Cell2011, Cell Metabolism 2012)以及蛋白质乙酰化调控肿瘤发生(Nature Communications 2017)等。代谢物和细胞周期信号对组蛋白乙酰化的调控加深了对乙酰化生理病理重要性的认识。
赵世民教授和生物医学研究院PI徐薇研究员为本研究共同通讯作者,赵世民课题组博士生张娇娇、毛云子,徐薇研究员课题组博士生樊婷婷为本文共同第一作者。